|
|
|
福島県教育センター所報ふくしま No.27(S51/1976.8) -006/026page
|
|
|
のを2等分し,一方の溶液にO.1NのNaOH溶液を数滴加えて,赤色溶液とする。
ポリエチレン製のスポイトでそれぞれの溶液をガラス管内に注入し冷水をかけると30秒程度で凝固する。この装置を写真-2のようにO・H・P上にセットする。
+(プラス)の容器には, NaOH水溶液(0.5N),+(プラス)側の容器にはH 2 S0 4 水溶液(O.5N)を入れ,両方の電極(ニッケル又は,ステンレス)に15〜20Vの電圧をかけ電解する。その結果,イオンはガラス管の中を異極に向って移動していく。電解と同時に,NaOH溶液にフェノールフタレインを加えて,アルカリ性にした赤色の寒天の+(プラス)極側から赤色の消失が起りH + の移動していることがスクリーンに映る。無色の寒天の方も―(マイナス)極側からOH - の移動により赤色になって動くのがわかる。電圧は前述のとおり15V程度でよいが,実際実験してみると,電流を150mA〜200mAにおさえる必要がある。200mA以上にすると,寒天がとけてしまって,いままで,やや不透明であったガラス管内が透明になりゲルの状態が保てなくなる。
図-3のAの部分は,赤色の消失がおこりBの部分は赤色になりながら矢印のように進行するがスケールで進行する速さを測定すると図-4のようなグラフになる。
両極に入れてあるH+とOH一あ濃度が同じなのにこのような結果になるのは,イオンの種類によって,移動速度がちがうためである。
中学校の段階では,移動速度のちがいについてはあまり深入りする必要はないが,この実験でもH+と0Hの移動速度のちがいは,はっきり確認できる。グラフに表わされた測定値と理論値とが完全に一致しないのは,
理論値は,無限大希釈度における当量伝導度から,算出したものであるが,この実験の場合は,ガラス管内の寒天の中にNa + とCl - が入っているためと,寒天の粘性低抗があるためなどが考えられる。
次の表は各イオンの電気伝導度であるが,これらの比は,イオンの移動速度の比とほぼ一致する。その理由は,電気伝導度Kは,抵抗をRとするとK=1/Rであるから, I=KV
水溶液の中の無限希釈当重イオン電導度(25 。 C)
陽イオン ohm -1 cm 陰イオン ohm -1 cm H + 349.8 OH - 198.3 Na + 50.10 Cl - 76.35 K + 73.50 1/2SO 4 2- 80.0 1/2Cu 2+ 55 1/2CO 3 2- 69.3 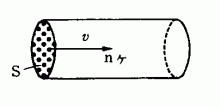
図-5図-5のように面積Sを単位体積中にあるn個のイオン(電荷をeとする)が,uの速度で移動しているものとすると,
となり,移動速度uは(s,n,eが一定ならば)イオンの電気伝導に比例するといってよい。すなわち上の表よりH + とOH - の移動速度の比は349.8/198.3=1.8程度である。
ところで,H + とOH - の電気伝導度が他のイオンに比べ異常に大きいことが目につく。これは,Na + やK + のようなH + とOH - 以外のイオンは,水の分子をかきわけながら移動するためイオン半径(正しくは水和半径)が小さいイオンの方が移動速度が大きい。
しかしH + とOH - は,水の分子をかきわけなから進むのではなく(したがってストークスの原理はあてはまらない。くわしくは,本センター所報No25,1Oぺ一ジ参照)ブロトン遷移による見かけの移動が起るためである。
この装置があれば,H + と0H - の移動だけでなく,有色のイオンの移動や,ガラス管内での化学反応なども観察できるわけである。授業の一助にしていただければ幸いである。
参考文献 化学実験事典 (講談杜) 科学の実験 (共立出版) 新中学校化学実験 (大日本図書)
|
|
|